人轮状病毒(HRV)是引起全世界婴幼儿严重急性胃肠炎和脱水的最主要病因,其发病原因是病毒感染小肠上皮细胞,从而造成细胞损伤引发腹泻,几乎所有儿童在出生后3-5年都感染过HRV,每年约有50多万名五岁以下儿童死于腹泻病。疾控中心估算在我国5岁以下儿童中,每年约发生轮状病毒腹泻1300万人次,每年轮状病毒腹泻门诊病例约250万人次,每年轮状病毒腹泻住院病例约23万人。我国轮状病毒发病致死率较高。在5岁以下儿童中,每10万人中就有3.5人会因轮状病毒死亡,死亡率是俄罗斯的6倍和巴西的3倍。轮状病毒疫苗在美国等发达国家已经被列为一类疫苗,由国家出资对所有儿童进行免费接种,美国接种率高达73%。轮状病毒疫苗在我国仍属于二类疫苗,由消费者自费接种,目前国内的接种率不足5%。轮状病毒疫苗共经历了三代技术发展,兰州所的单价轮状病毒疫苗采用的是第一代技术,直接将动物的轮状病毒培养后接种到人身上,效果不太好,国外已不再使用。发达国家使用的是第二代和第三代的轮状病毒疫苗。
轮状病毒疫苗技术发展趋势
轮状病毒疫苗技术发展趋势 | ||
- | 技术路径 | 代表产品 |
第一代 | 直接把动物的轮状病毒培养后接种到人身上,效果不太好,国外已不再使用 | 兰州所的罗威特 |
第二代 | 基因重配,动物和人的轮状病毒双感染,重新组合,然后接种 | 默沙东的Ratateq |
第三代 | 基因工程(DNA)疫苗,直接使用人的轮状病毒(DNA)进行接种 | GSK的Rotarix |
数据来源:公开资料整理
智研咨询发布的《2020-2026年中国五价轮状病毒疫苗行业市场竞争状况及投资前景预测报告》数据显示:兰州所为单价轮状病毒疫苗,只能预防G10P[12]血清型轮状病毒,而默沙东为口服轮状病毒五价活疫苗,适用于6-32周龄婴儿,以口服方式使用三剂,预防G1、G2、G3、G4及P1血清型所引发的轮状病毒肠胃炎。兰州所的单价轮状病毒疫苗和默沙东的五价轮状病毒疫苗均在国内获批上市。
不同轮状病毒疫苗比较
不同轮状病毒疫苗比较 | |||
疫苗 | 羊轮状病毒疫苗 | 基因重配5价人牛株轮状病毒疫苗 | 减毒人轮状病毒株疫苗 |
商品名 | 罗威特 | 轮达停 | 罗特律 |
生产商 | 兰州所 | 默克(默沙东) | 葛兰素史克 |
上市时间 | 2000年 | 2006年 | 2008年 |
剂量 | 4 | 3 | 2 |
抗原 | G10P[12] | G1,G2,G3,G4,P1A[8] | G1P[8] |
剂型 | 3ml | 2ml | 1ml |
价格 | 中标价172元/支 | 中标价280元/支 | 232美元/2剂 |
数据来源:公开资料整理
相比于发达国家和发展中国家(以金砖五国和部分亚洲国家为例),我国轮状病毒发病致死率较高。在5岁以下儿童中,每10万人中就有3.5人会因轮状病毒死亡,远高于其他发达国家。而与发展中国家相比,中国的死亡率是俄罗斯的6倍,巴西的3倍。针对婴幼儿感染轮状病毒,目前尚无特异治疗方法,有效的疫苗预防尤为重要。目前国际市场以GSK生产的单价轮状病毒疫苗Rotarix和默沙东生产的五价轮状病毒疫苗RotaTeq为主,我国兰州所生产的单价轮状病毒疫苗罗威特及越南Polyvac公司生产的Rotavin-M1疫苗均仅在本国销售。
全球已上市的主要轮状病毒疫苗信息对比
全球已上市的主要轮状病毒疫苗信息对比 | |||
疫苗 | 口服单价轮状病毒减毒活疫苗 | 口服五价重配轮状病毒减毒活疫苗 | 口服轮状病毒活疫苗 |
商品名 | Rotarix | RotaTeq | 罗威特 |
生产企业 | GSK | 默沙东 | 兰州所 |
上市时间 | 2005年墨西哥上市 | 2006年美国上市 | 2000年中国上市 |
2008年美国上市 | 2018年中国上市 | ||
剂型 | 1mL/剂 | 2mL/剂 | 3mL/剂 |
抗原 | G1P[8] | G1、G2、G3、G4、P1A[8] | G10P[12] |
适应症 | G1型和非G1型(G3、G4、G9)轮状病毒引起的肠胃炎 | G1-G4型及P1A[8]型轮状病毒引起的肠胃炎 | A群(G1-G4型)轮状病毒引起的腹泻 |
有效率 | 75%-85% | 75%-95% | 40%-60% |
适应人群 | 6周-24周婴幼儿 | 6周-32周婴幼儿 | 2月-3岁婴幼儿 |
接种程序 | 口服接种2剂,2、4月龄 | 口服接种3剂,2、4、6月龄 | 口服接种3剂,每年接种1剂 |
价格 | 美国91.05美元/剂 | 中国280元/剂 | 中国172元/剂 |
数据来源:公开资料整理
2018年全球已有91个国家将轮状病毒疫苗纳入国家免疫规划,6个国家将其纳入区域性免疫规划。随着婴幼儿轮状病毒腹泻越来越受到国际社会的重视,我们预计,未来将有更多国家将轮状病毒疫苗纳入国家免疫规划。
2018年全球轮状病毒疫苗国家免疫规划纳入情况

数据来源:公开资料整理
由于轮状病毒疫苗在许多国家尚未获批上市或者尚未纳入国家免疫规划,尤其是中国、印度等人口大国尚未将轮状病毒疫苗完全纳入免疫规划,全球新生儿童的轮状病毒疫苗可及率仅为47.5%。根据各国家轮状病毒疫苗接种率(无接种率数据的国家以百白破疫苗接种率数据代替)测算,2018年全球新生儿童轮状病毒疫苗接种率约为40.1%。在全球0.65亿轮状病毒疫苗覆盖的新生儿童中,平均接种率为0.546/0.646≈85%,这说明在轮状病毒疫苗在被纳入免疫规划后,各国家的接种率已处于较高水平。
2018年全球轮状病毒疫苗可及性分析
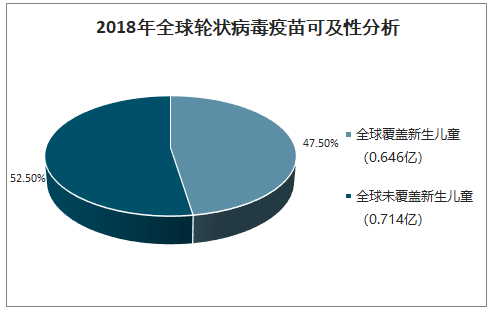
数据来源:公开资料整理
2018年全球轮状病毒疫苗接种率分析
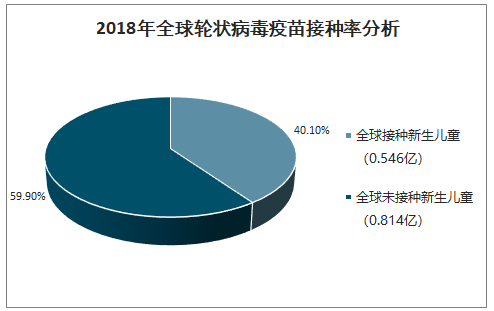
数据来源:公开资料整理
五价轮状病毒疫苗RotaTeq和单价轮状病毒疫苗Rotarix分别于2006年和2008年在美国获批上市,并分别于2007年和2009年被纳入美国国家免疫规划。2013年以来美国19-35月龄儿童的轮状病毒疫苗接种率达到70%以上,并基本维持稳定,2017年美国19-35月龄儿童的接种率为73.2%。自上市以来,全球轮状病毒疫苗销售额整体呈上升趋势,其中默沙东RotaTeq的销售达峰更快、后续销售额保持相对稳定,GSK的Rotarix销售达峰较慢、销售额持续较快增长。2018年默沙东的RotaTeq与GSK的Rotarix销售额分别为7.28亿和6.62亿美元,合计13.90亿美元。
2007-2018年全球主要轮状病毒疫苗销售额变化趋势
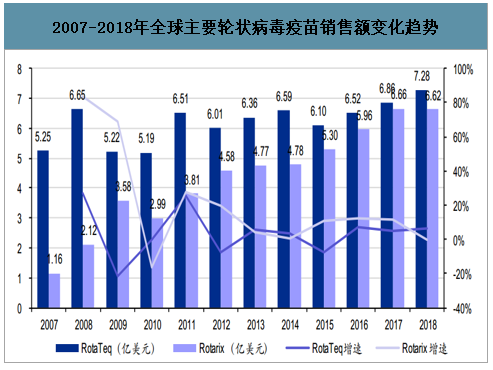
数据来源:公开资料整理
目前,国内上市的轮状病毒疫苗有兰州所的单价疫苗罗特威和默沙东的五价疫苗RotaTeq。其中,兰州所轮状病毒疫苗罗特威于2000年在国内获批上市,默沙东五价轮状病毒疫苗RotaTeq于2018年4月在国内获批上市,并于2018年9月首次批签发。
1)有效性和安全性优势明显
默沙东的五价轮状病毒疫苗RotaTeq于2008年10月17日经WHO认定为优先发展疫苗之一,截止2017年已在95个国家和地区投入使用,累计接种剂量近2.22亿剂次,为全球7900万婴幼儿提供保护,是全球使用最为广泛的轮状病毒疫苗之一。国外研究者JONESON曾针对RotaTeq的有效性和安全性做过为期2年的临床试验,试验包含了来自亚洲(孟加拉国和越南)和非洲(加纳、肯尼亚和马里)5个发展中国家的7500多例4-12周龄婴儿。试验结果表明:
1)有效性:亚洲1018例婴儿随机接受RotaTeq,接种疫苗后发生38例重症轮状病毒胃肠炎,发病率为3.7%;非洲2733例婴儿随机接受RotaTeq,接种疫苗后发生79例重症轮状病毒胃肠炎,发病率为2.9%。
2)安全性:亚洲和非洲婴儿发生严重不良事件(包括上呼吸道感染、腹泻、呕吐、发热、中耳炎、激惹和咳嗽等)的比例分别为2.5%和1.5%。国产轮状病毒疫苗罗特威在不同地区的多次临床观察数据显示,接种疫苗后儿童仍然发病的概率均值为6.53%,产生上呼吸道感染、腹泻、呕吐、发热等不良反应的概率均值为4.51%。虽然并不是头对头临床试验,但从一定程度上反映出,五价轮状病毒疫苗RotaTeq有效性和安全性优于国产单价疫苗。此外,五价轮状病毒疫苗RotaTeq的有效率为75%-95%,而国产轮状病毒疫苗罗特威的有效率仅为40%-60%。
2)儿童接种依从度优势明显
根据推荐接种程序,五价轮状病毒疫苗RotaTeq的适应人群为6周-32周婴幼儿,接种程序为2月龄、4月龄、6月龄依次口服接种3剂,接种周期为4个月;兰州所轮状病毒疫苗罗特威的适应人群为2月-3岁婴幼儿,接种程序为口服接种3剂,每年接种1剂,接种周期为2年。因此,五价轮状病毒疫苗RotaTeq的接种周期明显短于国产疫苗,儿童接种的跑针、漏针现象将大幅减少,儿童接种依从度优势明显。
3)未来市场竞争格局良好
目前国内多家企业正在开展多价轮状病毒疫苗的研发工作,目前研发进度最快的是兰州所的III价轮状病毒基因重配疫苗,已于2016年11月申报生产,但目前仍处于补充材料阶段,距离上市仍需一定时间;武汉所的口服六价重配轮状病毒活疫苗(Vero细胞)处于III期临床阶段;而GSK已主动撤回人类轮状病毒减毒活疫苗的上市申请。因此,从国内企业的研发进度来看,未来几年国内轮状病毒疫苗的市场竞争格局都将较为良好。
我国轮状病毒疫苗研发进度
我国轮状病毒疫苗研发进度 | |||||
药品名称 | 受理号 | 申请类型 | 企业名称 | 办理状态 | 状态开始日 |
Ⅲ价轮状病毒基因重配疫苗 | CXSS1600009 | 新药 | 兰州所 | 上市申请 | 2016年11月 |
人类轮状病毒减毒活疫苗 | JXSS1200009 | 进口 | GSK | 上市申请撤回 | 2015年9月 |
口服六价重配轮状病毒活疫苗(Vero细胞) | CXSL1300002 | 新药 | 武汉所 | III期临床 | 2018年5月 |
口服轮状病毒活疫苗 | CXSR1500001 | 复审 | 鑫科贤 | 获批临床 | 2016年11月 |
冻干四价口服轮状病毒活疫苗(FRhL-2细胞) | CXSL1600031 | 新药 | 博沃生物 | 获批临床 | 2018年12月 |
轮状病毒灭活疫苗(Vero细胞) | CXSL1600129 | 新药 | 昆明所 | 申报临床 | 2017年2月 |
数据来源:公开资料整理
4)国内接种率依旧较低、提升空间大
2018年我国国产轮状病毒疫苗罗特威与五价轮状病毒疫苗RotaTeq的批签发量分别为515万和79万支,以中标价分别为172元/支和280元/支测算,国内轮状病毒疫苗市场规模约11亿元。2018年我国出生人口1523万人,按轮状病毒疫苗3支/人份测算,2018年我国轮状病毒疫苗的接种率仅13%,远低于美国和全球平均水平。
2011-2019年10月我国轮状病毒疫苗批签发量(万支)

数据来源:公开资料整理
2019年1-10月我国五价轮状病毒疫苗RotaTeq的批签发量已达到344万支,预计全年批签发量将达到400-500万支。由于五价轮状病毒疫苗RotaTeq的保护率更高、安全性更好、且接种周期更短,因此我们预计,未来五价轮状病毒疫苗RotaTeq有望对国产单价疫苗形成明显市场替代,并进一步扩容市场。参考国内Hib系列疫苗40%左右的接种率,以未来每年新生人口1500万人,单价和五价轮状病毒疫苗的接种率分别为5%和25%测算,预计我国轮状病毒疫苗市场空间约35亿元,其中五价轮状疫苗RotaTeq的市场空间约31.5亿元。
我国轮状病毒疫苗市场空间测算
我国轮状病毒疫苗市场空间测算 | ||||||
疫苗 | 新生人口(万人) | 假设接种率 | 疫苗需求(万支) | 中标价(元/支) | 市场空间(亿元) | 总市场空间(亿元) |
单价轮状疫苗 | 1500 | 5.00% | 225 | 172 | 3.87 | 35.37 |
五价轮状疫苗 | 25.00% | 1125 | 280 | 31.5 | ||
数据来源:公开资料整理

 公众号
公众号
 小程序
小程序
 微信咨询
微信咨询

















![研判2025!中国消弧线圈成套装置行业产业链、发展现状、竞争格局及发展趋势分析:智能电网建设持续推进,市场需求稳步增长[图]](http://img.chyxx.com/images/2022/0408/55d853aceb464ffcf6fad7c27bbd7795797b1b5a.png?x-oss-process=style/w320)
![研判2025!中国二氟二苯甲酮行业产业链、发展现状、竞争格局及发展趋势分析:产能高度集中[图]](http://img.chyxx.com/images/2022/0330/d1363a7ee3953fc25ed09e0b79158acce9dc7c22.png?x-oss-process=style/w320)
![2025年中国汽车数字化营销行业发展现状分析及未来发展趋势研判:“营销运营化”是汽车行业在新形势下营销突围方向,未来将更加智能化、个性化和多元化[图]](http://img.chyxx.com/images/2022/0330/ff5315f651f3e124d0f5a156ac51655e46e5433f.png?x-oss-process=style/w320)
![研判2025!中国网络视频版权保护行业发展历程、市场规模及重点企业分析:技术革新与政策护航双轮驱动,5G与元宇宙拓展未来新空间[图]](http://img.chyxx.com/images/2022/0330/ce25a2275c336b52d58303ed80fb7924b3fd1022.png?x-oss-process=style/w320)
![研判2025!中国特种印刷行业相关政策、产业链、市场规模、重点企业及未来前景分析:特种印刷市场持续扩张,绿色转型趋势显著[图]](http://img.chyxx.com/images/2022/0330/920e1a3ff3bb6b7f469fbaa1e9ad45bc470a7578.png?x-oss-process=style/w320)
![研判2025!中国油套管行业产业链、发展现状、竞争格局及发展趋势分析:下游行业拉动下,油套管前景可期[图]](http://img.chyxx.com/images/2022/0330/b388a599ab8b82a70e79838a8b0d600efa11727f.png?x-oss-process=style/w320)